弱いのに酒を飲むのは遺伝子のせい? 食道癌リスクとの関連も明らかに 約17万6千人のゲノム解析
日本人約17万6千人を対象にしたゲノム解析により、飲酒行動に影響を与える遺伝的要因が同定され、アルコールに弱いにもかかわらず飲酒量が多い人に特徴的な遺伝的構造のあることが明らかになった。愛知県がんセンターと名古屋大学の研究グループによるものであり、米国科学振興協会のジャーナル「Science Advances」に論文が掲載されるとともに、各機関のサイトにプレスリリースが掲載された。アルコールの分解に関わる酵素であるALDH2遺伝子(ALDH2)の遺伝的な違いがあり、これは食道癌のリスクとも一部関連があることから、この知見が食道癌の個別化予防に役立つことが期待されるという。

研究の概要:飲酒の量だけでなく、「飲酒行動」も遺伝子が影響?
これまでの研究で、人がどれだけアルコールを飲むか(飲酒習慣や量)は遺伝によっても影響を受けることがわかっている。摂取後のアルコールは主にアルコール脱水素酵素によりアセトアルデヒド※1に分解され、アセトアルデヒドはさらにアルデヒド脱水素酵素(aldehyde dehydrogenase;ALDH)、とくにALDH2により無害な酢酸に分解される。
※1 アセトアルデヒド:アルコールの最初の代謝産物。飲酒したあとのフラッシング反応(顔が赤くなる、頭痛、動悸、吐き気など)を引き起こすだけでなく、ヒトへの発癌性が示唆されている。ヒトの体内では主にALDH2酵素により酢酸へと代謝され無毒化される。
ALDH2の遺伝子(ALDH2)には、アセトアルデヒドの分解能力に差をもたらす遺伝的な違いがあり、この遺伝的な違いによって日本人は三つのグループに分けることができる。アセトアルデヒドの分解能力が低い場合、アルコールを飲むとアセトアルデヒドが体内にたまり顔が赤くなるフラッシング反応※2が起きるため、このALDH2の遺伝的な違いはアルコールに強い人、弱い人、全く飲めない人の違いをもたらす主な要因ともなっている。
※2 フラッシング反応:少量の飲酒で、顔が赤くなる、頭痛、動悸、吐き気などが起こること。アセトアルデヒドが蓄積されることが主な原因となって起こる。
研究グループでは、日本分子疫学コンソーシアム(J-CGE)※3、ながはまコホート※4およびバイオバンク・ジャパン※5で収集された日本人集団約17万6千人を対象に、ALDH2の遺伝的な違いとの組み合わせによって飲酒行動に影響を与える、別の遺伝的要因を探索するゲノム解析を行った。
※3 日本分子疫学コンソーシアム(J-CGE):J-CGEはJapanese Consortium of Genetic Epidemiology studiesの略。日本の分子疫学研究を統合し、遺伝情報を利用して疫学研究を行うコンソーシアム。本研究にはJ-CGEとして以下、四つの分子疫学研究が含まれている。多目的コホート研究(JPHC Study)…国立癌研究センターを中心に、1990年より実施されているコホート研究。日本各地の約14万人を対象に、生活習慣や生活環境と疾病の発症について追跡を行っている。愛知県癌センター病院疫学研究(HERPACC)…愛知県癌センターにおいて1988年より実施されている病院疫学研究。初診患者を対象に生活習慣に関するアンケート調査と、臨床情報および血液サンプルの収集を行っている。日本多施設共同コーホート研究(J-MICC Study)…2005年より日本全国の複数の研究機関が協力して実施しているコホート研究。10万人以上の日本人集団を対象に、血液サンプルの収集、生活習慣および癌やその他の生活習慣病の発症について追跡を行っている。東北メディカル・メガバンク計画(TMM)…東北大学東北メディカル・メガバンク機構と岩手医科大学いわて東北メディカル・メガバンク機構が2013年より実施しているプロジェクト。東北地方の約15万人を対象にコホート研究を実施し、生体試料や生活習慣および健康情報を収集したバイオバンクを構築している。
※4 ながはまコホート:2007年より滋賀県長浜市で実施されているゲノム・コホート研究。地域住民を対象に、遺伝情報の登録、健康診断やアンケート調査による健康状態や生活習慣の追跡を行っている。
※5 バイオバンク・ジャパン:日本における大規模なバイオバンク(生体試料バイオバンク)プロジェクト。日本国内の複数の病院や医療機関と連携し、2003年から2018年までの間に日本人集団27万人分のゲノムDNAや血清サンプルおよび臨床情報などが収集された。
その結果、七つの遺伝子領域にみられた遺伝的要因が、ALDH2の遺伝的な違いと組み合わさることで飲酒行動に影響を与えることをつきとめた。つまり、ALDH2の遺伝的な違いではアルコールに弱いタイプの人でも、別の遺伝的要因との組み合わせによっては、よりたくさんアルコールを飲んでしまうということ。
さらに、本研究で同定された遺伝子領域の遺伝的要因の中には、ALDH2の遺伝的な違いとの組み合わせにより、代表的な飲酒関連癌である食道癌のリスクをより高める要因が存在することがわかった。
これらの研究結果は、日本人の遺伝的背景に基づいた個別化予防のさらなる促進につながることが期待される。
研究の背景:アルコールを「少し飲める」人は飲酒行動が癌リスクを左右
飲酒はさまざまな疾患や障害に関連する。アルコールの代謝に関わる酵素、ALDH2の遺伝子(ALDH2)には、日本人の飲酒行動に最も強力な影響を与える遺伝的要因となる、重要な遺伝的な違い(バリアント※6)が存在する。その重要なバリアントは、ALDH2遺伝子上の特定の場所にある一つの塩基がGからAに変化する一塩基多型(SNP)※7で、「rs671」※8と呼ばれている。
※6 バリアント:ゲノムDNAの塩基配列や構造の違いにより、遺伝情報の一部は人によって異なっており、この違いをバリアントと呼ぶ。とくに、塩基配列中の一つの塩基が他の塩基に変わる変化で、一般集団でよく見られるものを一塩基多型(SNP)と呼ぶ※7。ALDH2の酵素活性に大きな影響のあるALDH2遺伝子上のSNPとしてrs671※8が知られており、塩基配列がグアニン(G)からアデニン(A)に変化する。遺伝子は原則的に父由来と母由来の二つで一組であることから、GとAの組み合わせにより、それぞれの人は3種類の遺伝型(GG型、GA型、AA型)のいずれかを持つ。
※7 一塩基多型(SNP):SNPはSingle Nucleotide Polymorphismの略。バリアントのうち、ゲノムDNAの塩基配列中の一つの塩基が他の塩基に変わることによるものを指す。
※8 rs671:ALDH2のバリアントの中でALDH2の酵素活性に大きな影響のあるSNP。ALDH2遺伝子の塩基配列の特定の箇所でグアニン(G)がアデニン(A)に置き換わり、504番目のアミノ酸がグルタミン酸からリシンに置き換わることで、ALDH2酵素活性が大きく低下し、アセトアルデヒドの分解ができなくなる。
rs671により、日本人は、GG型、GA型、AA型という三つの遺伝型に分けられ、どの遺伝型を持つかによって飲酒行動に明確な違いがある。GG型の場合、アセトアルデヒドを代謝できるため飲酒後のフラッシング反応が起こりにくく、飲酒する傾向にある。欧米系集団ではほとんどがこのGG型。一方、AA型はアセトアルデヒドの分解能力が極めて低くほぼ飲酒しない。中間のGA型はGG型よりアセトアルデヒドの分解能力が低いものの、人によって幅広い飲酒パターンを示す。
この遺伝型による飲酒行動の違いは、頭頸部癌や食道癌などの飲酒関連癌のリスクにも大きく寄与する。飲酒してもアセトアルデヒドが蓄積しにくいGG型と飲酒をしないAA型は飲酒関連癌のリスクが低いのに対し、GA型は飲酒によるアセトアルデヒド曝露量の上昇に伴い飲酒関連癌の最も高いリスクを有する(Koyanagi YN, et al. Eur J Cancer Prev. 2017)。このため、GA型の幅広い飲酒行動を決定する別の遺伝的要因の同定は、飲酒関連癌の個別化予防に寄与すると考えられる。
研究内容と成果:少し飲める遺伝子+よく飲む遺伝子=食道癌リスク増大
本研究はまず、J-CGE、ながはまコホート及びバイオバンク・ジャパンより収集された日本人集団17万5,672人の遺伝情報と飲酒行動の情報を用いて、日本人のゲノム全体の中からALDH2 rs671の遺伝型にかかわらず、飲酒行動に関連するバリアントを探すゲノムワイド関連解析(GWAS)※9を行った(層別なし解析)。
※9 ゲノムワイド関連解析(GWAS):GWASはGenome-Wide Association Studyの略。人々の遺伝的な違いが特定の形質(健康状態や身体の特徴)とどのように関連しているのかを調べる研究方法。数百万カ所のバリアントを全ゲノム(遺伝情報の全体)にわたって網羅的に調査し、それらが特定の形質と関連しているかどうかを検討する。
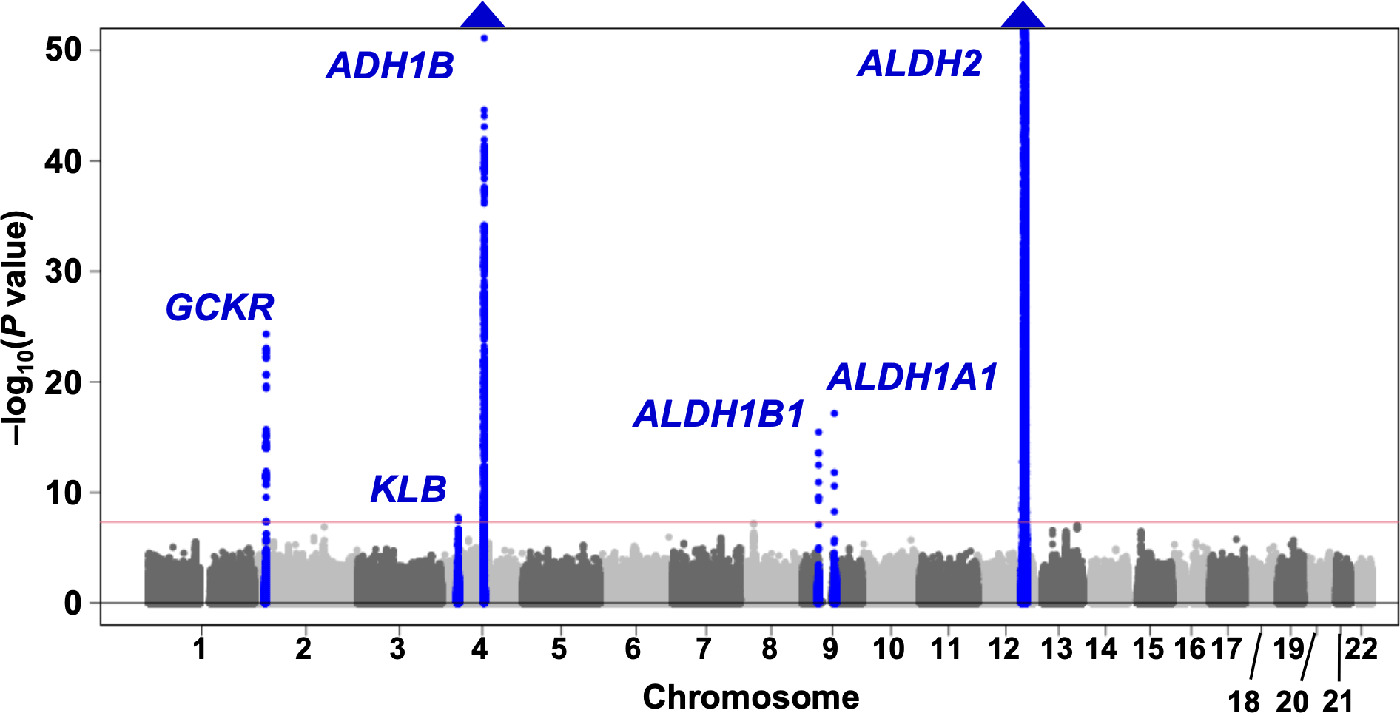
その結果、ALDH2を含む六つの遺伝子領域(GCKR遺伝子、KLB遺伝子、ADH1B遺伝子、ALDH1B1遺伝子、ALDH1A1遺伝子、ALDH2遺伝子)上のSNPが飲酒関連バリアントとして同定された(図1)。
図1 1日アルコール摂取量のGWASのマンハッタンプロット(層別なし解析)
次に、それぞれのrs671遺伝型別にGWASを行った(層別あり解析)。AA型は対象者のほとんどが飲酒を全くしないためAA型のみのGWASは行わなかった。
層別あり解析の結果、GG型では三つの遺伝子領域(GCKR遺伝子、KLB遺伝子、ADH1B遺伝子)上のSNPが飲酒関連バリアントとして同定された(図2A)。これらはrs671遺伝型がほとんどGG型である欧米系集団を対象とした飲酒行動GWASでよく検出される遺伝子領域と一致した。
一方で、GA型ではアルコール代謝関連遺伝子であるADH1B、ALDH1B1、ALDH1A1、ALDH2遺伝子を含む六つの遺伝子領域(GCKR遺伝子、ADH1B遺伝子、ALDH1B1遺伝子、ALDH1A1遺伝子、ALDH2遺伝子、GOT2遺伝子)上のSNPが飲酒関連バリアントとして同定された(図2B)。
図2 1日アルコール摂取量のGWASのマンハッタンプロット(層別あり解析)
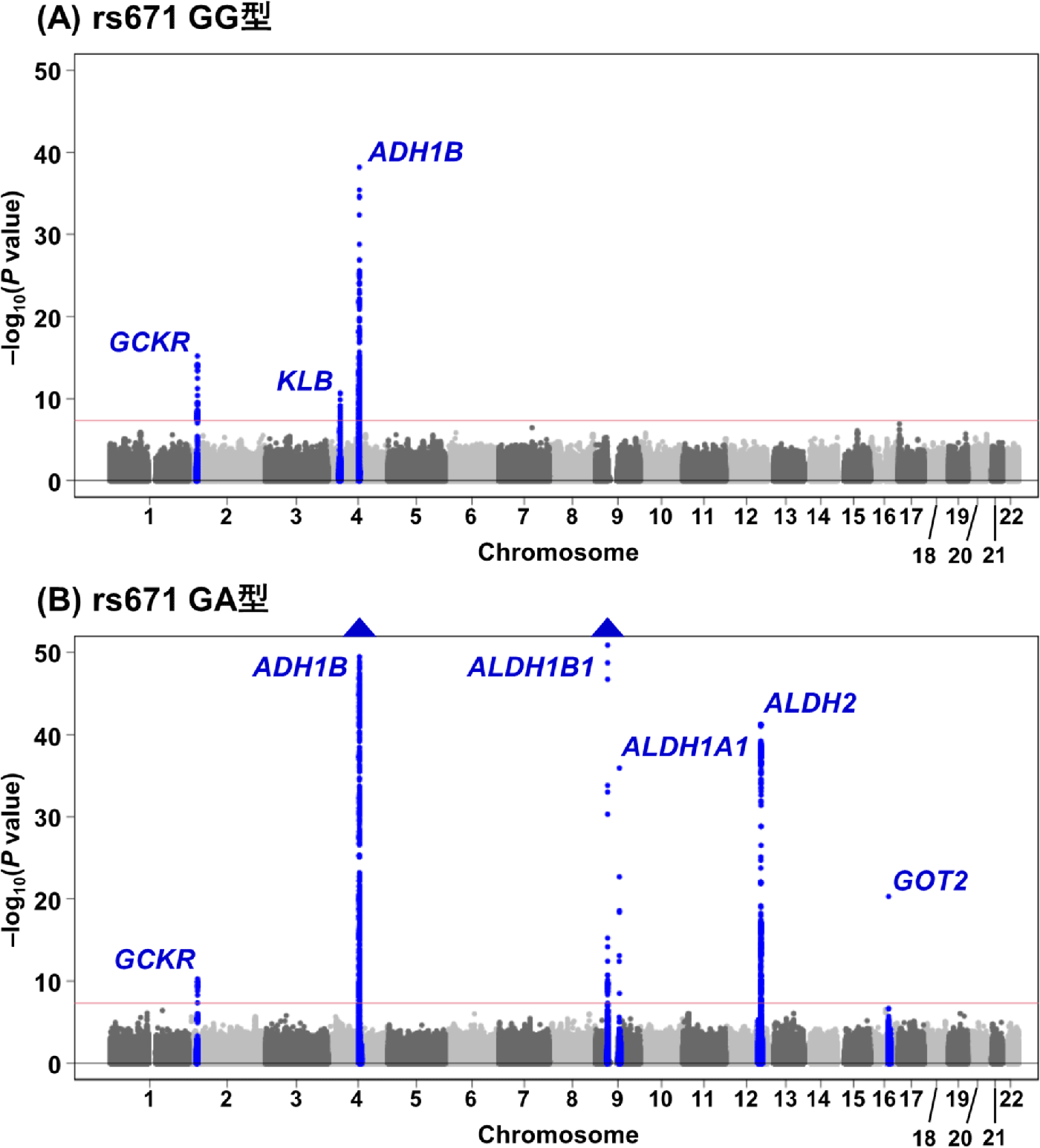
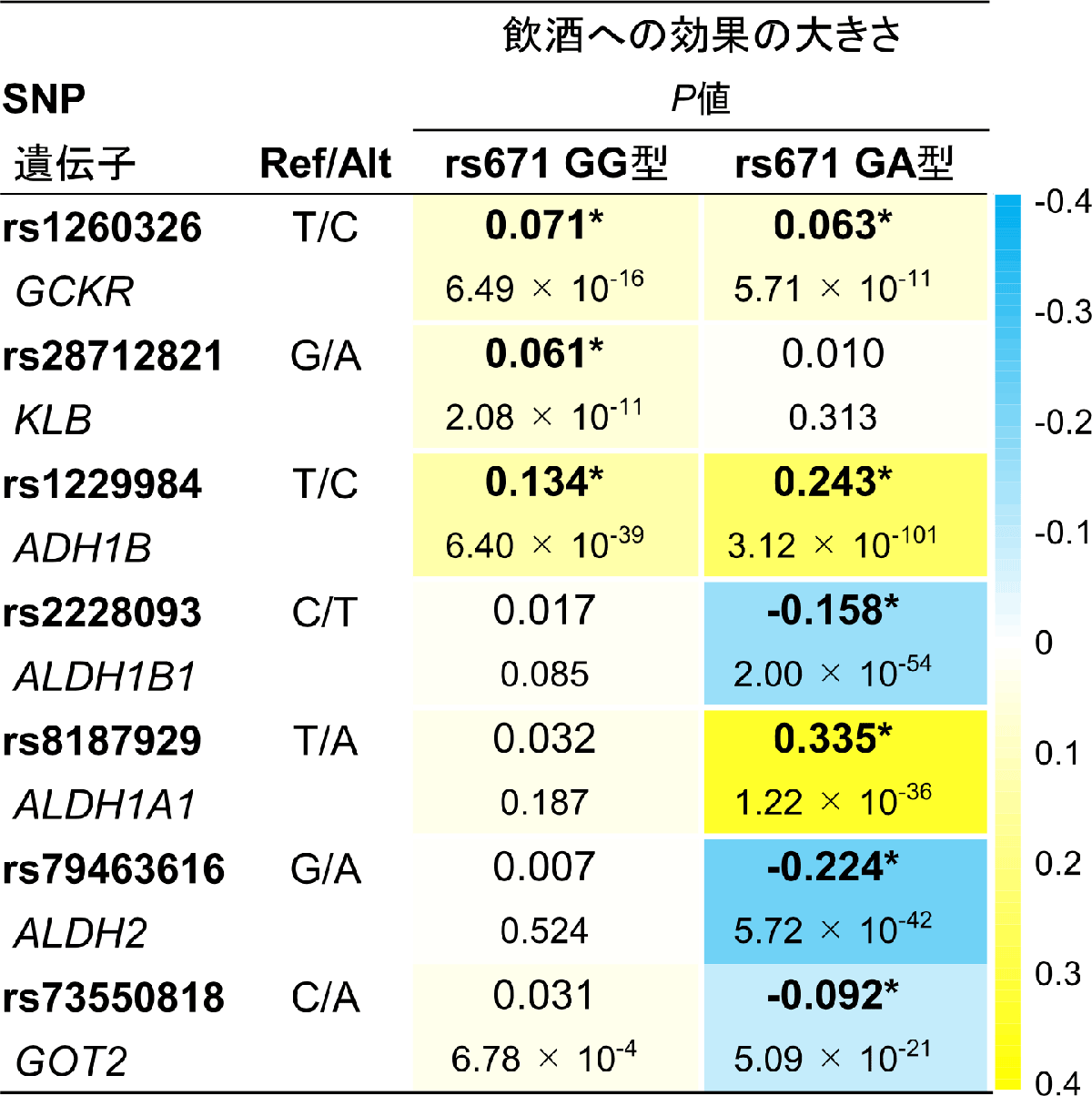
図3は、層別あり解析により同定された遺伝子領域で最も関連の高いSNPの飲酒への効果の大きさを示している。各SNPの飲酒への効果の大きさは、rs671遺伝型の違いにより大きく異なっていた。例えば、ALDH1A1 rs8187929はALDH1A1遺伝子上の一つの塩基がTからAのバリアントに変化するSNPだが、rs671 GG型の人がALDH1A1 rs8187929にA塩基(TA型やAA型)を持っていても飲酒量は変わらないのに対し、rs671 GA型の人がALDH1A1 rs8187929にA塩基を持つと飲酒量が増える。
図3 層別あり解析で同定されたSNPの飲酒量への効果量
このようにrs671遺伝型で層別化したGWASを行うことで、遺伝型によって表現型※10(今回の場合は飲酒量)への影響が異なるSNPが明らかになり、SNPが単独ではなく複数組み合わさって表現型に影響している(交互作用※11という)ことが示された。
※10 表現型:個体の見た目や機能など、遺伝子と環境の影響を受けて個体がもつ形態や機能の特徴を「形質」といい、個々の個体で観察できる形質タイプを「表現型」という。例えば、「身長」、「ABO式血液型」、「目の色」の各形質に対して、「高い・低い」、「A型・B型・AB型・O型」、「青色・緑色・黒」などが表現型として観察される。
※11 交互作用:異なる要因同士が組み合わさることによって、単独での効果とは異なる効果を生み出すこと。
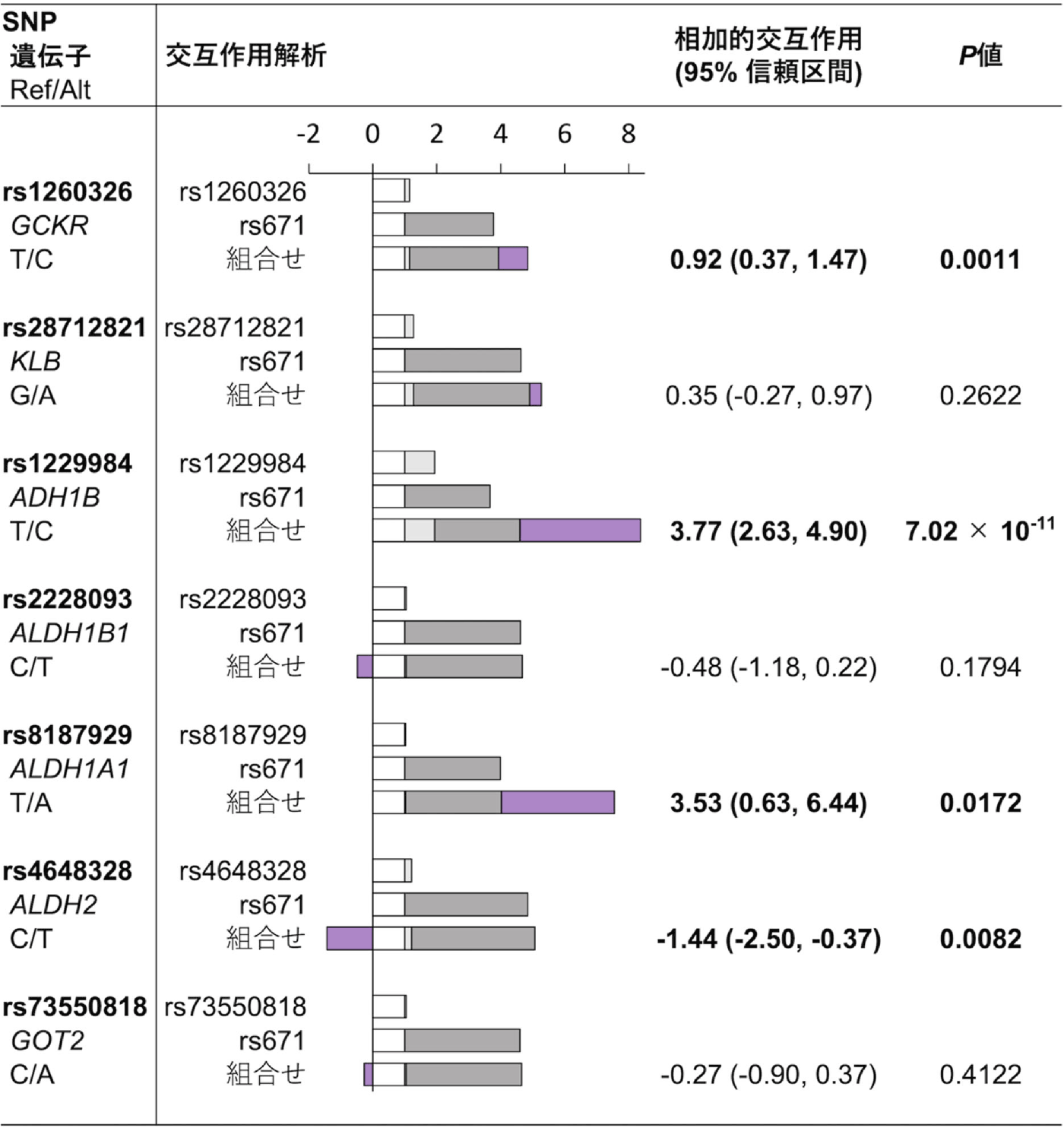
さらに、層別あり解析で同定された七つのSNPと代表的な飲酒関連疾患である食道癌リスクとの関連を検討するため、愛知県がんセンター病院疫学研究(HERPACC)とバイオバンク・ジャパンにより収集された食道癌症例群と非癌対照群を用いた食道癌症例対照研究を行った。その結果、層別あり解析で同定された七つのSNPのうち四つが食道癌リスクに対してもrs671と「交互作用」を伴って関連していることが示唆された(図4)。
例えば、ADH1B rs122994はADH1B遺伝子上の一つの塩基がTからCのバリアントに変化するSNPだが、rs671 GA型の人が、ADH1B rs122994にC塩基を持つと、それぞれ単独でのリスクを足し合わせた場合より食道癌のリスクが3.77倍上乗せされて高くなる。
図4 層別あり解析で同定されたSNPとrs671を組み合わせて算出した食道癌リスク
今後の展望:遺伝的背景に基づいた飲酒関連癌の個別化予防へ
今回の研究結果から、飲酒行動の遺伝的背景には、rs671と複数のSNPが「交互作用」を伴い関与していることが示された。このように、「遺伝型層別GWAS」を用いた研究アプローチは、表現型に対して強力な影響を持つSNPがある場合、このSNPと交互作用を発揮する新規SNPを検出するための有効な手法であると考えられる。層別あり解析で同定されたSNPには、飲酒行動だけでなく食道癌リスクにもrs671と「交互作用」を伴い関与するものが存在しており、日本人の遺伝的背景に基づく飲酒関連癌の個別化予防のさらなる促進に寄与することが期待される。
プレスリリース
「お酒に弱いはずなのに飲んでしまうのはなぜ?」 日本人の飲酒行動を決定づける遺伝的構造の解明と食道がんリスクとの関連(名古屋大学)
文献情報
原題のタイトルは、「Genetic architecture of alcohol consumption identified by a genotype-stratified GWAS, and impact on esophageal cancer risk in Japanese people」。〔Sci Adv. 2024 Jan 26;10(4):eade2780〕
原文はこちら(American Association for the Advancement of Science)





















 熱中症予防情報
熱中症予防情報 SNDJユニフォーム注文受付中!
SNDJユニフォーム注文受付中!











